

走进人生就是博-尊龙凯时
NEWS自身免疫病新纪元:尊龙凯时ADC技术重塑市场格局
来源:裘河梵 日期:2025-07-17由于ADC独特的抗体、连接子与毒素三重结构设计,其通过抗原介导的内化作用有效释放毒素,诱发肿瘤细胞凋亡,同时利用旁观者效应杀伤邻近肿瘤细胞,从而在提高疗效的同时降低系统毒性,ADC迅速崛起为肿瘤治疗的核心动力。全球已有19款ADC获批上市,证实其在肿瘤治疗中的重要性。目前,约40款处于临床Ⅲ期,超过300款在临床Ⅰ或Ⅱ期,标志着ADC将在未来几年迎来爆发期。
目前已上市的ADC靶点覆盖CD33、CD30、CD22、HER2、CD79b、Nectin4、TROP2等13种靶点。在Ⅲ期研究中,虽然HER2仍是热门靶点,但新靶点如HER3、B7H3、B7H4等逐渐显现出发展潜力,分别占比10%(4/40)。在适应症方面,已上市的ADC中有7款针对血液肿瘤,12款针对实体瘤,如乳腺癌和胃癌。Ⅲ期临床管线多集中在实体瘤,仅有3款针对血液肿瘤。
ADC的发展呈现出“纵向深耕与横向拓展”的趋势:深入挖掘现有靶点的适应症潜力,同时针对稀有肿瘤及难治性癌症的创新突破。ADC的特异性和稳定性不断增强,其适应症正向非肿瘤领域扩展,例如B7H3 ADC在骨肉瘤中的应用和CD3/CD7 ADC在移植物抗宿主病的研究等。
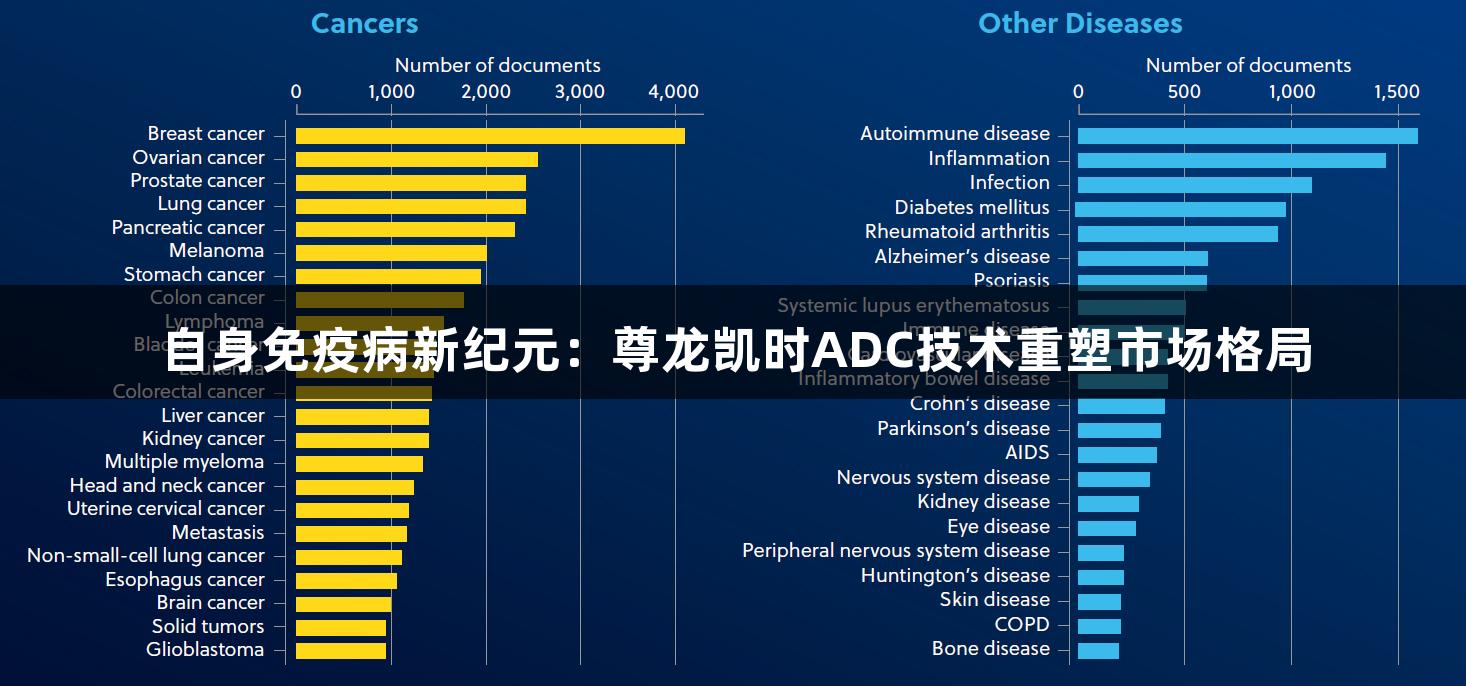
自免疫疾病的治疗历史是一部“疗效与安全”的平衡探索史。早在1948年,梅奥诊所的医生首次为类风湿关节炎患者注射类固醇,取得显著疗效。但随之而来的骨质疏松与感染风险也成为临床痛点。虽然TNF单抗和IL-6抑制剂部分缓解了毒性问题,但其应答率不足50%。全球依然有超过5亿自免患者面临无效治疗的困境。
ADC技术为自免疫疾病的治疗提供了新思路。自免ADC的设计旨在精准调控免疫细胞,而不是仅仅杀伤靶细胞。通过靶向识别过度活化的免疫细胞,将类固醇、siRNA等免疫调节有效载荷递送至病灶,减少全身暴露,从而避免传统广谱抑制剂带来的全身性副作用。
靶向TNF、IL-6等可溶性细胞因子可能导致免疫抑制,因此ADC需选择特异性抗原进行靶向,例如BDCA2/CLEC4C作为浆细胞样树突状细胞的标志物,为系统性红斑狼疮(SLE)治疗提供新方向。CD19作为B细胞的标志物,与多种自免疾病的发展密切相关。
在自免ADC领域,艾伯维作为先行者开发了ABBV-3373,一个靶向阿达木单抗(TNF)的ADC产品。尽管其在Ⅱ期临床中展现出较好的疗效,但由于成药性问题,此项目最终被终止。相应地,艾伯维升级推出了ABBV-154,通过抗体偶联新型载荷,尽管具有更高的治疗潜力,但相应的高糖皮质激素暴露使其也遭遇了开发难题。
在中国,Biotech则通过“新靶点+新载荷”的创新策略,逐步由追随者转变为行业引领者。映恩生物研发的DB-2304靶向BDCA2,同时释放激素类似物,力求在高效免疫调节且减少系统性糖皮质激素暴露方面实现突破。2025年计划获得NMPA临床批件,适应症为SLE。先声药业开发的SIM0708则是结合了IL-4Rα抗体与糖皮质激素载荷,展现出抑制B细胞活化的强大效能,未来有望成为新一代安全有效的自免药物。
然而,自免ADC的前景广阔,却依然面临“靶点选择、载荷设计和长效安全性”的挑战。随着技术的发展与临床数据的积累,ADC在非肿瘤领域同样将迎来突破,尤其是在自免领域。自免ADC的革命才刚刚开始,不仅将重塑千亿市场的格局,还将为自免患者带来“治愈的希望”。
人生就是博—尊龙凯时为客户提供全面的ADC药物研发与生产解决方案,全力助您加速研发进程!
全国客户服务热线
15838762555
总部地址:沈阳高明区都街道14号